|
3.5. EFFETS SECONDAIRES DU TRAITEMENT DU CANCER DE LA PROSTATE. |
3.5.1. LES PRINCIPAUX EFFETS SECONDAIRES.
|
|
- Incontinence urinaire :
L'incontinence urinaire est l'impossibilité
de contrôler les urines, et entraîne des fuites urinaires.
La chirurgie prostatique, en
particulier la prostatectomie totale, peut endommager le sphincter.
- En
cas de fuites persistantes par insuffisance du tonus du sphincter, une
rééducation sphinctérienne est indiquée. En cas d’échec, la mise en place
d’un sphincter artificiel
(sphincter AMS 800®), ou d’une
bandelette sous urétrale (type INVANCE®) est une solution efficace.
- Parfois, l’incontinence se fait par
« regorgement » car elle est due à la mauvaise évacuation de la vessie,
habituellement par du tissu tumoral ou cicatriciel qui bloque l'évacuation
vésicale. Les fuites surviennent donc par "trop plein". Le traitement est
celui de l'obstruction.
- Les fuites par impériosités mictionnelles
(envies pressantes) surviennent particulièrement après radiothérapie,
quand la tolérance de la vessie au remplissage est diminuée.
-
Impuissance :
L'impuissance est définie par l'impossibilité à
obtenir une érection. Les nerfs érecteurs peuvent être endommagés par la
chirurgie prostatique et/ou la radiothérapie.
Différents traitements existent :
Le citrate de sildénafil (VIAGRA®) et les autres médicaments similaires (CIALIS®,
LEVITRA®, SPEDRA@) peuvent permettre de récupérer des érections après le
traitement du cancer de la prostate.
Les injections intra caverneuses de prostaglandine E1 (une substance produite naturellement dans
l'organisme, qui déclenche l'érection, et que le patient peut injecter
directement, de façon indolore, à la base du pénis, 5 à 10 minutes avant
le rapport) (EDEX®, CAVERJECT®) sont utilisées, et parfois dès la période
post opératoire, pour favoriser le retours des érections spontanées.
Les gels intra-urétraux de PGE1 sont également disponibles (MUSE®, VITAROS®)
Les prothèses péniennes ne sont quasiment plus utilisées (implants
péniens) |
|
|
|
Retour au sommaire |
|
3.5.2. EFFETS SECONDAIRES DE LA PROSTATECTOMIE TOTALE.
|
|
Les effets secondaires essentiels sont l'incontinence urinaire et l'impuissance. Le contrôle normal de la continence urinaire revient habituellement 2 à 3 mois après la prostatectomie totale, mais un certain degré d'incontinence urinaire d'effort peut persister de façon permanente. Si l'incontinence urinaire demeure gênante après une rééducation bien faite, un traitement par mise en place d'un sphincter artificiel (ou bandelette) peut être indiqué.
Après prostatectomie totale, une impuissance est habituellement observée dans les premiers mois suivant l'intervention. Les chances de récupérer des érections sont liées à l'âge du patient, à la préservation des nerfs érecteurs et au stade de la maladie. Après prostatectomie totale, 40% à 90% des patients sont impuissants.
|
|
Retour au sommaire |
|
3.5.3. EFFETS SECONDAIRES DE LA RADIOTHERAPIE.
|
|
La radiothérapie externe peut entraîner des troubles intestinaux (diarrhée, colite), et des troubles urinaires survenant essentiellement pendant le traitement (fréquence urinaire, diminution du jet, envies pressantes, brûlures en urinant, présence de sang dans les urines). La radiothérapie peut engendrer une certaine fatigue en cours de traitement. Environ 40 à 60% des patients traités par radiothérapie externe ont des troubles de l'érection, ces troubles pouvant débuter même plusieurs mois après la fin du traitement. |
|
La curiethérapie a des effets secondaires très limités, n'entraînant aucune incontinence et des troubles de l'érection dans 10 à 15% des cas. |
|
Retour au sommaire |
|
3.5.4. EFFETS SECONDAIRES DU TRAITEMENT HORMONAL.
|
|
Après traitement hormonal, 90% des hommes ont une diminution ou une disparition de la libido (désir sexuel) et une impuissance. Certains patients ont des bouffées de chaleur qui disparaissent généralement après quelques mois. Dans certains cas, il peut y avoir un gonflement et une sensibilité des seins. |
|
Certains anti-androgènes peuvent entraîner des effets secondaires (diarrhée, difficultés respiratoires, troubles de l'accommodation visuelle …). Le traitement hormonal à long terme peut entraîner une ostéoporose avec fragilisation osseuse. |
|
Retour au sommaire |
|
3.6. CANCER DE LA PROSTATE : LES DIFFERENTS STADES.
|
|
Le "stade" du cancer de la prostate indique le degré d'extension du cancer dans la prostate, aux tissus avoisinants et aux autres organes. Le stade détermine en grande partie le type de traitement utilisé et permet, associé à d'autres éléments, de prédire le pronostic de la maladie. Le stade de la maladie est habituellement défini par un système appelé "le système TNM" qui décrit l'extension de la tumeur primitive (T), l'absence ou la présence de métastases ganglionnaires (N), et l'absence ou la présence de métastases à distance (M). |
|
Le stade clinique est déterminé par le toucher rectal, les biopsies, l'échographie endorectale et l'IRM avec antenne endorectale.
|
|
Le stade pathologique est basé sur l'examen au microscope de la prostate et des ganglions enlevés au cours de l'intervention chirurgicale. |
|
Le stade clinique est donc utilisé pour prendre les décisions thérapeutiques mais il peut sous-estimer le stade réel de la maladie car l'extension réelle, en particulier si elle est microscopique, peut échapper aux examens préopératoires. Le stade pathologique, déterminé par l'examen au microscope de la prostate enlevée chirurgicalement, est plus précis et permet de prédire en partie la survie. Le stade pathologique n'est donc pas déterminé chez les patients qui n'ont pas de prostatectomie totale. |
|
|
Stade T : |
|
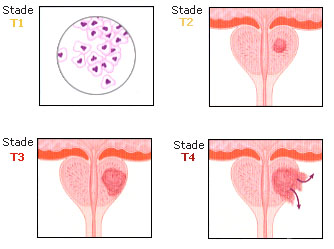
Il y a 4 catégories qui décrivent le stade T. |
|
|
T1 correspond à une tumeur non perçue au toucher rectal. T1a et T1b correspondent à des cancers découverts incidemment lors de l'examen du tissu prostatique obtenu au cours d'une intervention pour adénome bénin de la prostate. Ces cancers sont donc découverts "par accident" et représentent moins de 5% (T1a) ou plus de 5% (T1b) du tissu prostatique enlevé. T1c correspond à des cancers découverts par biopsies faites en raison d'une élévation suspecte du taux de PSA. |
|
|
T2 correspond à un cancer palpable au toucher rectal et qui semble localisé à la glande, intéressant un seul (T2a) ou les 2 lobes (T2b) de la prostate. |
|
|
T3 correspond à un cancer qui s'étend en dehors de la prostate et/ou aux vésicules séminales (T3b). |
|
T4 correspond à un cancer qui a envahi les organes adjacents à la prostate (vessie, rectum, muscle). |
|
|
Stade N : |
|
N0 correspond à l'absence d'envahissement lymphatique, et N1 à l'envahissement d'un ou de plusieurs ganglions du petit bassin. |
|
|
Stade M : |
|
M0 correspond à l'absence de métastases à distance et M1 à la présence de métastases en dehors du petit bassin (os, poumons, foie ou cerveau). |
|
Retour au sommaire |
|
3.7. COMMENT CHOISIR LE TRAITEMENT LE PLUS ADAPTE STADE PAR STADE ?
|
|
Le stade du cancer est l'un des principaux facteurs pour choisir le type de traitement, mais la décision doit être prise individuellement, pour chaque patient, en fonction de son âge, de son état de santé, de ses objectifs et de son sentiment vis à vis des effets secondaires éventuels. Les patients les plus âgés ou ceux ayant une autre affection grave peuvent choisir un traitement qui va simplement éviter les symptômes et les complications, et choisir la surveillance ou le traitement hormonal. La radiothérapie permet d'obtenir des résultats équivalents à la prostatectomie totale à 5 ou 10 ans.
A l'inverse, les patients les plus jeunes vont devoir envisager les résultats du traitement à 10 ou 20 ans et envisager un traitement vraiment curateur tout en tenant compte des effets secondaires éventuels.
Ces décisions difficiles nécessitent une discussion franche et ouverte avec votre médecin traitant, votre urologue, voire un autre spécialiste (seconde opinion) ou la rencontre avec des patients ayant déjà eu ce type de traitement proposé.
Ces recommandations vont vous permettre de mieux comprendre les problèmes que posent le cancer de la prostate et les conseils de votre médecin. Nous vous conseillons d'en discuter avec votre médecin et de lui poser les questions suivantes :
Quelle est l'influence de mon âge, de mon état de santé général et de mes autres maladies éventuelles sur le choix du traitement du cancer de la prostate ?
Quel est le stade (classification TNM) de mon cancer et comment ce stade influe-t-il sur le choix du traitement ?
Comment le score de Gleason de mon cancer et le taux sanguin de PSA (antigène spécifique prostatique) permettent-ils de prédire la survie et de choisir le traitement le plus adapté ?
Quels sont les effets secondaires du traitement proposé et quelle influence ont-ils sur ma qualité de vie ultérieure ?
Comment peut-on traiter les effets secondaires du traitement proposé ?
Décider du traitement du cancer de la prostate.
Options thérapeutiques stade par stade :
Stade T1a (cancer découvert par résection de la prostate):
Comme le cancer de la prostate de stade T1a tend à se développer extrêmement lentement, aucun traitement immédiat n'est généralement recommandé à moins que le patient n'ait des symptômes, une espérance de vie de plus de 20 ans, un score de Gleason supérieur à 6 ou un taux de PSA supérieur à 1 ng/ml après la résection prostatique.
Stades T1b, T1c, T2a et T2b :
Ces stades sont considérés ensembles vis à vis du traitement ; et le choix du traitement dépend du score de Gleason et de l'espérance de vie. Dans ces cancers localisés, sans extension en dehors de la prostate, le traitement est fait dans un but curatif, pour guérir, et il peut s'agir soit d'une prostatectomie totale soit d'une radiothérapie ou d'une curiethérapie. L'ablation de la prostate (prostatectomie totale) est en règle réservée aux patients en bonne santé, ayant une espérance de vie supérieure ou égale à 10 ans (donc en pratique âgés de moins de 70 ans), qui ont une tumeur localisée à la prostate.
La curiethérapie donne les mêmes résultats à long terme que la prostatectomie totale, en cas de cancer localisé de bas risque. Les patients dont l'espérance de vie est limitée peuvent choisir un traitement différé ou la radiothérapie externe.
Le curage ganglionnaire a pour but de déceler un envahissement des ganglions et éviter une prostatectomie totale qui serait inutile dans ce cas.
En cas de cancer résiduel après prostatectomie totale, généralement détecté par une élévation du taux de PSA postopératoire, une radiothérapie externe adjuvante (généralement 3 à 4 mois après l'intervention chirurgicale, quand la continence a été récupérée) peut être indiquée.
Stades T3a, T3b, T4N0, TXN1-3 et TXM1 :
Généralement, les patients ayant une extension extra prostatique de la tumeur, même limitée, sont traités par radiothérapie externe (avec ou sans traitement hormonal avant le début de la radiothérapie). La prostatectomie, si elle est faite dans un tel cas, doit être généralement complétée par une radiothérapie complémentaire.
En cas de métastases à distance, un traitement local (chirurgie ou radiothérapie) est inutile, et un traitement hormonal est recommandé car il permet de bloquer les cellules prostatiques quelque soit l'endroit du corps où elles se trouvent.
|
|
Retour au sommaire |
|
3.8. AUTRES TRAITEMENTS
|
|
- Ablatherm® : C'est un système de
traitement du cancer de la prostate par ultrasons focalisés par voie
endorectale. L'absorption soudaine et intense des ultrasons au point
focal, entraîne une augmentation brutale de la température (environ 85°C)
qui aboutit à une nécrose irréversible du tissu dans la zone focale. Les
ultrasons focalisés sont utilisés de façon encore expérimentale dans le
traitement de certains cancers de la prostate. D'après les dernières
communications scientifiques, ce traitement serait réservé aux patients
inopérables, et donc indiqué à titre palliatif, en particulier après échec
de la radiothérapie. Les complications rapportées sont les suivantes :
impuissance dans 77 % des cas, disparition de l'éjaculation dans 97 % des
cas, rétrécissement du col vésical 14 % des cas, et nécessité d'un
traitement chirurgical complémentaire dans 20 % des cas. Dans les cancers
localisés de bas grade, le taux de récidive tumorale est élevé, évalué à
15% des 18 mois après le traitement.
Focal One®
Focal One® est un système de
traitement à ultrasons focalisés conçu pour le traitement focal du cancer
de la prostate. Il associe des technologies permettant de localiser, viser
et traiter des foyers de cancer dans la prostate. Un système de fusion
élastique d’image autorise le traitement de cibles vues à l’échographie
per-opératoire après importation des images de l’IRM pré-opératoire.
Dans l’étude pilote (1)
portant sur 10 patients ayant un cancer T1 ou T2a, tous les patients
avaient des biopsies négatives dans la zone traitée 30 jours après le
traitement. Aucune incontinence n’était rapportée, mais 20% des patients
avaient une diminution des érections.
Dans la série récente portant sur 101 patients traités et ayant eu des biopsies de contrôle, le taux
de survie sans traitement radical à 2 ans a été de 89% (2). A 1 an, 97% et
78% des patients avaient conservé une continence et des érections
normales, respectivement. Il faut souligner que ’objectif principal
n’était pas la disparition du cancer, mais seulement l’absence de cancer
dit significatif (score de Gleason
³ 7, ou longueur de cancer > 3 mm quel que
soit le score, ou > 2 carottes positives).
Les détracteurs de ces
techniques par ultrasons focalisés soulignent le fait qu’elles paraissent
surtout efficaces chez les patients qui ne nécessitent probablement aucun
traitement mais une simple surveillance… La FDA n’a pas approuvé
l’utilisation des ultrasons localisés dans le traitement du cancer de la
prostate en raison du manque de
preuves de l’efficacité de cette technique.
1
Gelet A., Crouzet S., Rouviere O. et al.
Focal treatment of prostate cancer using Focal One
device: pilot study results. J Ther Ultrasound, 2015:3 (Suppl 1): O54
2
Rischmann P., Gelet A., Riche B. et al.
Focal high intensity focused ultrasound of unilateral
localized prostate cancer: A prospective multicentric hemiablation study
of 111 patients. Eur Urol. 2017, 71: 267-273
-
Cryochirurgie : Cette technique détruit les cellules cancéreuses
par congélation brutale et répétée de la prostate à l'aide d'une sonde
refroidissante (azote liquide) introduite sous anesthésie dans la
prostate. Actuellement, cette technique a été utilisée expérimentalement
en cas de récidive du cancer après radiothérapie. L'efficacité de cette
technique n'est pas encore démontrée mais des complications graves peuvent
survenir : obstruction vésicale, incontinence urinaire, impuissance et
lésions rectales
|
|
Retour au sommaire |
|
3.9. Que faire après échec du traitement initial ?
|
|
La sous-estimation du stade réel de la maladie est fréquente, surtout en l'absence d'IRM endorectale avant prostatectomie totale ou curiethérapie. Après prostatectomie totale, en cas d'extension du cancer au-delà de la capsule prostatique ou dans les vésicules séminales, ou si le taux de PSA ne devient pas indétectable ou remonte après un certain délai, et si la récidive paraît uniquement locale, on peut proposer une radiothérapie, dite "adjuvante" qui peut diminuer le risque de progression locale. L'effet de la radiothérapie adjuvante sur la survie reste controversée. La radiothérapie adjuvante est habituellement faite au moins 3 à 4 mois après la prostatectomie, après récupération d'une continence urinaire satisfaisante. |
|
En cas de récidive après radiothérapie, une prostatectomie totale peut parfois être indiquée mais la récidive n'est locale que dans moins de 10% des cas, et la prostatectomie totale après radiothérapie entraîne fréquemment des complications. Cette prostatectomie totale "de sauvetage" n'est donc pas habituellement recommandée. |
|
Retour au sommaire |
|
|
4. ADENOME DE LA PROSTATE. |
|
L'adénome de la prostate, ou hyperplasie bénigne de la prostate (HBP), est une maladie fréquente dont l'incidence (la fréquence dans la population) augmente avec l'âge. C'est de cette affection dont parle souvent les patients en disant qu'ils "ont la prostate". En effet, elle affecte 50 à 75 % des hommes de plus de 50 ans, et la moitié des hommes de 60 ans ont des troubles urinaires en rapport avec une hyperplasie bénigne de la prostate. En 2010, 40 % de la population française aura plus de 60 ans et de plus en plus de patients vont donc consulter pour des troubles urinaires liés à un adénome prostatique. |
|
L'hyperplasie bénigne de la prostate associe une prolifération des cellules prostatiques et l'augmentation progressive du volume de la prostate qui entraîne une obstruction du jet urinaire. |
|
L'adénome est une maladie bénigne, indépendante du cancer : elle ne dégénère pas en cancer, mais peut coexister dans la prostate avec un cancer. |
|
Retour au sommaire |
|
4.1. Le développement de LA PROSTATE.
|
|
La prostate est faite de différents types cellulaires. Les cellules épithéliales forment la portion glandulaire de la prostate et les cellules stromales le tissu conjonctif et musculaire. Le développement de la prostate est sous l'influence de la testostérone. L'augmentation progressive du volume de la prostate par le développement d'une hyperplasie (adénome) bénigne à partir de l'âge de 40 ou 50 ans est vraisemblablement sous contrôle hormonal, mais le mécanisme exact est encore inconnu. Le finastéride (Chibro-Proscar®) agit sur les cellules épithéliales et diminue le volume de ces cellules et donc de la prostate. Les a bloquants agissent sur les cellules musculaires lisses du stroma, en diminuent le tonus et n'ont pas d'effet sur les cellules épithéliales. |
|
L'augmentation du volume de la prostate avec l'âge est un phénomène normal. |
|
Une première augmentation de volume survient à la puberté : la prostate double de volume à ce moment là. |
|
Vers l'âge de 25 ans, la glande recommence à grossir progressivement mais les symptômes sont rares avant 40 ans. La moitié des hommes de 60 ans et 90% des hommes de 70 à 80 ans ont des symptômes urinaires liés à une augmentation du volume de la prostate. Cette augmentation bénigne de la prostate avec l'âge est appelée hyperplasie bénigne de la prostate, ou hypertrophie prostatique, ou adénome. |
|
Retour au sommaire |
|
4.2. EVOLUTION DE L’ADENOME.
|
|
Le processus prend des années et évolue de façon très progressive. |
|
Le développement de la prostate est sous l'influence des androgènes. |
| Le mécanisme initial de l'HBP est inconnu, probablement un déséquilibre entre androgènes et œstrogènes au niveau prostatique. La quantité de DHT (dihydrotestostérone) intraprostatique, le dérivé actif de la testostérone, parait un élément primordial de la croissance prostatique. Le déficit congénital en 5 a -réductase, l'enzyme qui produit la DHT à partir de la testostérone, empêche le développement de la prostate. |
| Les symptômes liés à l'adénome évoluent de façon lente et insidieuse sur plusieurs années. |
|
Quand la prostate augmente de volume, elle tente à comprimer l'urètre et gêne ainsi la vidange normale de la vessie. Ce mauvais fonctionnement se traduit par des symptômes : diminution de la force du jet, jet intermittent, difficultés à démarrer le jet, envies pressantes d'uriner, gouttes retardataires, envies fréquentes d'uriner en particulier la nuit. Au début, la diminution de la force du jet est surtout perceptible le matin au réveil ou après s'être retenu pendant longtemps. La paroi de la vessie devient plus épaisse (vessie de lutte) et tolère moins bien le remplissage entraînant des envies d'uriner fréquentes et une mauvaise vidange de la vessie. |
| L'obstacle à la vidange vésicale est d'abord bien compensé par la contraction du détrusor, puis entraîne une phase d'hypertrophie du détrusor, puis une phase de décompensation avec un détrusor atone, un résidu post-mictionnel important avec distension de la vessie et des reins. |
|
|
Le traitement doit intervenir avant que la vessie et les reins ne se détériorent de façon irréversible. |
|
Le volume de la prostate n'a pas d'influence directe sur la gravité des symptômes. Certains hommes avec une prostate très volumineuse ont peu de symptômes tandis que d'autres avec une prostate peu volumineuse vont être très gênés. Cela est probablement dû à la différence de composition de l'adénome qui peut être plus ou moins glandulaire ou plus ou moins fibreux. Le volume de la prostate ou l'augmentation du volume ne sont donc pas à eux seuls des facteurs de gravité de la maladie, et ne sont pas des arguments pour décider un traitement ou une intervention. |
|
Parfois, les symptômes sont minimes jusqu'à la survenue d'un blocage complet et brutal avec impossibilité complète d'uriner malgré une envie pressante. Cette "rétention aiguë des urines" peut survenir sans cause particulière ou être déclenchée par la prise de certains médicaments (en particulier gouttes nasales en hiver). |
|
Parfois, l'adénome de la prostate peut causer des problèmes plus sérieux: infections urinaires, dilatation rénale avec insuffisance rénale, calculs vésicaux, incontinence urinaire, distension vésicale. Le traitement doit être suffisamment précoce pour éviter le passage à ces complications. |
|
Si la rétention aiguë des urines est l'indication d'un traitement chirurgical, cet épisode ultime de l'évolution de la symptomatologie de l'HBP est en fait assez rare, avec une incidence cumulée sur dix ans de 4 à 73 %. |
|
L'existence de troubles mictionnels, la diminution du débit urinaire, l'augmentation du volume de la prostate et l'âge sont des facteurs associés avec un risque accru de rétention aiguë des urines dans la population générale. |
|
Retour au sommaire |
|
4.3. DIAGNOSTIC.
|
|
L'adénome de la prostate est tellement fréquent, et les symptômes tellement banals et tellement bien connus que le patient fait habituellement le diagnostic lui-même et vient consulter pour "la prostate". Le médecin fait alors le diagnostic par un interrogatoire, un examen et des tests peu douloureux destinés à confirmer la présence d'un adénome, évaluer ses conséquences éventuelles (symptômes, obstruction de l'évacuation vésicale, altération de la qualité de vie…) et décider d'un éventuel traitement. |
|
Retour au sommaire |
|
4.3.1. LES SYMPTÔMES LIES A L'ADENOME.
|
|
L'HBP entraîne des symptômes obstructifs |
|
dysurie initiale, |
|
jet intermittent, |
|
jet faible de petit calibre, |
|
gouttes retardataires, |
|
et des symptômes irritatifs |
|
pollakiurie diurne et nocturne, |
|
impériosités. |
|
(La prédominance de symptômes irritatifs doit faire rechercher une autre cause que l'HBP). |
|
|
L'obstruction peut entraîner : |
|
une trabéculation vésicale |
|
des diverticules vésicaux, |
|
un retentissement d'amont avec hydronéphrose pouvant aboutir à |
|
une insuffisance rénale, |
|
une infection urinaire du fait de la stase, |
|
la formation de calculs vésicaux, |
|
une hématurie, |
|
une incontinence par des " mictions " par regorgement ; |
|
voire une rétention aiguë des urines parfois révélatrice. |
|
Des symptômes non urinaires, mais liés aux conséquences de l'obstruction (poussée abdominale lors des mictions), peuvent exister : |
|
hernie inguinale, hémorroïdes. |
|
Les symptômes urinaires, souvent liés à une banale HBP à partir d'un certain âge, doivent cependant faire rechercher d'autres causes de troubles mictionnels. |
|
|
|
En pratique clinique, du fait de sa grande prévalence, l'hyperplasie bénigne de la prostate est habituellement un diagnostic de présomption: |
|
- quand un homme de plus de 50 ans se plaint d'un ou de plusieurs des symptômes évocateurs |
|
- quand la prostate est souple et augmentée de volume au toucher rectal, |
|
- quand il n'y a pas d'autre cause pouvant expliquer les symptômes (maladie du col, tumeur de vessie, infection, rétrécissement urétral, cancer de la prostate, troubles neurologiques...) |
|
|
Les examens doivent permettre d'éliminer un cancer de la prostate car on sait que les deux pathologies, adénome et cancer, peuvent coexister dans la prostate. |
|
Retour au sommaire |
|
4.3.2. COMMENT FAIT-ON LE DIAGNOSTIC D'ADENOME ?
|
|
Selon les bonnes pratiques cliniques, tout patient de plus de 50 ans consultant son médecin pour des troubles mictionnels doit avoir au minimum : |
|
1/ - un interrogatoire, qui évalue les symptômes : qualité du jet, nombre de levers nocturnes, éventuelles fuites ou envies pressantes (impériosités), présence d'infection urinaire et/ou de sang dans les urines (hématurie); et le retentissement des symptômes sur la vie quotidienne. L'interrogatoire recherche des problèmes neurologiques qui pourraient avoir des répercussions urinaires: antécédent d'accident vasculaire cérébral, de maladie de Parkinson, de traumatisme de la colonne vertébrale... |
|
|
2/ - un "score symptomatique" : c'est un questionnaire rempli par le patient, surtout utilisé dans les protocoles, qui permet d'apprécier la gravité des symptômes. Score total côté de 0 à 35. |
|
3/ - un examen physique : examen des organes génitaux externes, recherche d'une hernie. Recherche d'une distension de la vessie au-dessus du pubis. Toucher rectal permettant de préciser la taille, la consistance, la symétrie de la prostate. L'adénome se traduit par une prostate augmentée de volume, de consistance souple. Tout nodule palpable ferme ou dur est suspect, et 50 % environ sont des cancers. |
|
4/ - une échographie vésico-prostatique |
|
L'échographie vésico-prostatique a remplacé l'urographie (la radiographie des reins faite après une injection d'iode) comme examen initial. |
|
L'échographie permet d'évaluer le volume de la prostate, la vidange vésicale et l'état des reins. L'échographie prostatique est habituellement faite par voie sus-pubienne, à la partie basse de l'abdomen, mais peut également être faite par voie endorectale pour mieux analyser la structure interne de la glande. L'aspect normal de la prostate en échographie est hétérogène. |
|
|
En cas d'adénome, l'échographie peut simplement être faite par voie sus-pubienne ( à la partie basse de l'abdomen comme chez la femme enceinte), et détermine le volume prostatique (en cc), la régularité de la paroi vésicale, l'absence de tumeur vésicale visible et de calcul vésical, le volume du résidu post-mictionnel (volume d'urine restant dans la vessie après avoir fait uriner le patient). L'échographie peut détecter un résidu post-mictionnel même minime, de l'ordre de 15 à 20 cc. Le résidu est en général surestimé par l'échographie du fait de la distension vésicale qu'on fait habituellement subir au patient pour le temps prostatique de l'échographie. En pratique, on estime qu'un résidu post-mictionnel est vraiment anormal au-dessus de 100 cc. |
|
|
L'échographie transrectale n'a qu'une indication : guider les biopsies en cas d'induration au toucher rectal et/ou d'élévation du taux de PSA. |
|
5/ - un dosage de la créatininémie : |
|
Il permet de détecter une insuffisance rénale. L'adénome de la prostate peut entraîner une insuffisance rénale s'il existe une obstruction avec un résidu post-mictionnel notable, et une dilatation du haut appareil au-dessus de cette vessie qui se vide mal. La mise en place d'une sonde vésicale permettant d'abaisser la créatininémie apporte la preuve de l'origine prostatique de l'insuffisance rénale. |
|
6/-un ECBU (examen cyto-bactériologique des urines): recherche la présence de sang dans les urines, et/ou une infection urinaire. |
|
7/- une débitmétrie est parfois faite: Une débitmétrie est réalisée quand le patient urine dans un appareil appelé débitmètre. Cet appareil automatique mesure la durée de la miction, le volume uriné, le débit maximal et le débit moyen |
|
8/- un dosage du PSA (antigène spécifique prostatique) |
|
L’utilisation du dosage du PSA dans le sang a révolutionné la prise en charge du cancer de la prostate. Mis en évidence pour la première fois dans le liquide séminal en 1971, l’antigène spécifique prostatique (PSA) est une protéine produite exclusivement par les cellules prostatiques. Le rôle du PSA, qui est une enzyme, est de participer directement à la liquéfaction du sperme après l'éjaculation. |
|
Le PSA est spécifique du tissu prostatique mais il n'est pas spécifique du cancer de la prostate. |
|
Les valeurs seuils de la normale sont définies statistiquement pour chaque méthode de dosage du PSA, et n’ont qu'une valeur indicative. |
|
La limite supérieure de la normale est souvent égale à 4 ng/ml. En pratique, les patients ayant un taux de PSA > 10 ng/ml vont avoir de toutes façons une échographie prostatique endorectale avec des biopsies échoguidées à la recherche d'un foyer cancéreux ; tandis que les patients ayant un taux de PSA < 4 ng/ml et un toucher rectal normal vont être considérés comme ayant un simple adénome. |
|
Le problème essentiel concerne les patients ayant un taux de PSA compris entre 4 et 10 ng/ml. En effet, de nombreux hommes vus en urologie ont un taux de PSA compris entre 4,1 et 10 ng/ml, avec une prostate augmentée de volume mais souple au toucher rectal. |
|
Le dilemme est alors de savoir à qui proposer des biopsies prostatiques sous échographie, sachant que 25 % seulement d'entre eux ont un cancer de la prostate. |
|
Pour améliorer la valeur prédictive du PSA à ces taux intermédiaires, différents moyens ont été proposés, mais le concept le plus récent, le ratio PSA libre/PSA total, repose sur le fait que le PSA dans le sang circule en grande partie lié à des inhibiteurs des protéases, l' a 1 antichymotrypsine (PSA-ACT) et l' a 2 macroglobuline (PSA-AMG). Des tests permettent de doser séparément le PSA total, le PSA lié à l' a chymotrypsine et le PSA libre. La proportion de PSA libre est plus basse en cas de cancer de la prostate qu'en cas d'adénome, et le dosage simultané des différentes formes de PSA peut aider à distinguer entre adénome prostatique et cancer. |
|
Les résultats préliminaires montrent qu'un % PSA libre diminué correspond à un risque élevé de cancer. La probabilité de cancer est de 59 % en cas de % PSA libre < 10, et de 10 % en cas de % PSA libre > 26 %. |
|
Ainsi, l'utilisation d'un seuil limite de 15% (biopsie faite si PSA libre < 15%) pour le pourcentage de PSA libre < 15 % permettrait de détecter au moins 90 % des cancers tout en évitant plus de 30 % des biopsies négatives, donc superflues, chez des patients ayant un taux intermédiaire de PSA. |
|
|
9/- D'autres examens complémentaires appropriés sont parfois prescrits, en particulier pour éliminer une autre cause de troubles urinaires si les symptômes paraissent atypiques : |
|
- en cas d'hématurie (sang dans les urines) : Urographie intraveineuse, échographie rénale, fibroscopie vésicale, cytologie urinaire (tumeur de vessie? tumeur du rein?) |
|
- en cas de symptômes irritatifs prédominants : fibroscopie vésicale, cytologie urinaire, examen urodynamique (tumeur vésicale?, instabilité vésicale ?) |
|
- en cas de faiblesse du jet (dysurie) isolée : urétrographie, fibroscopie vésicale (rétrécissement urétral ?) |
|
- en cas d'insuffisance rénale : échographie rénale (dilatation des cavités ?) |
|
Retour au sommaire |
|
4.3.3. Autres causes de troubles mictionnels EN DEHORS DE L'ADENOME.
|
| Obstructives : |
|
- anomalie du col vésical: soit maladie du col, observée chez des sujets jeunes ayant une obstruction cervico-prostatique sans augmentation du volume de la prostate ; soit sclérose post-opératoire du col vésical. On appelle maladie du col la maladie observée chez des sujets jeunes où l'on a une obstruction de l'évacuation vésicale, sans que la prostate soit vraiment augmentée de volume |
|
- cancer de la prostate (souvent associé à HBP) |
|
- rétrécissement de l'urètre |
|
- rétrécissement du méat urétral |
|
- valve de l'urètre (nouveau né et enfant mâles) |
|
- corps étranger |
| Fonctionnelles : |
|
- anomalie du muscle vésical (neurologique, musculaire) |
|
- rétention médicamenteuse ( alpha-stimulants, en particulier gouttes nasales en hiver) |
|
- instabilité du muscle vésical |
|
- trouble psychogène : défaut de relaxation du col vésical lors de la |
|
miction, sans sténose, en particulier chez les hommes de 30-45 ans anxieux ou stressés. |
| Infectieuses et tumorales : |
|
- cystite |
|
- tumeur de vessie, y compris carcinome in-situ (CIS) |
|
- prostatite (infection de la prostate), abcès prostatique |
|
Retour au sommaire |
|
4.4. LES TRAITEMENTS.
|
|
L'adénome est une maladie bénigne qui affecte la qualité de la vie mais pas sa durée. La gêne causée par les symptômes est l'élément fondamental qui incite à consulter en vue d'un traitement, et la plupart des traitements sont donc indiqués dans le but de soulager les symptômes. L'évolution de l'adénome chez un patient donné est imprévisible et le concept de chirurgie préventive ne peut être fondé,
Parmi les français âgés de 50 à 80 ans sans antécédents chirurgicaux prostatiques, seuls 18,8 % n'ont aucun symptôme urinaire. Dans cette tranche d’âge, 6,9 % des hommes ont été opérés pour adénome. On estime qu'un homme de 50 ans, a un risque d'environ 15 % d'avoir une intervention chirurgicale pour adénome avant l'âge de 80 ans. Ainsi, l'opération n'est pas inéluctable, et la proportion d'hommes opérés n'est que de 1 %, 7 % et 19 % dans les groupes à 50 à 59 ans, 60 à 69 ans et plus de 70 ans respectivement.
On estime que 65.000 interventions chirurgicales pour adénome de la prostate sont faites chaque année en France, et 69 % de ces interventions sont faites par voie endoscopique. Parmi les patients opérés, 88 % sont satisfaits du résultat de l'intervention.
Il y a 3 groupes de traitements:
Les Traitements Chirurgicaux
- incision cervico-prostatique (ICP)
- résection transurétrale de la prostate (RTUP) : classique, ou avec courant bipolaire, ou par laser…
- chirurgie ouverte
Les Traitements invasifs alternatifs
- thermothérapie (PROSTATRON?)
- micro-ondes (TUNA®, PROSTIVA®)
- "stents"
Les Traitements médicaux
- extraits de plantes
- a bloquants
- inhibiteurs de la 5 alpha réductase
|
|
Retour au sommaire |
|
4.4.1. TRAITEMENT CHIRURGICAL.
|
4.4.1.1. Incision cervico-prostatique.
|
|
Il s'agit de l'incision transurétrale du col vésical et de la prostate. Cette intervention est simple, rapide, et permet le plus souvent de conserver une éjaculation normale. Elle est particulièrement faite chez les sujets jeunes (< 60 ans), ayant une obstruction liée à une petite prostate (< 30 g) avec un PSA normal. |
|
Retour au sommaire |
|
4.4.1.2. Résection endoscopique de prostate.
|
|
C'est actuellement la technique chirurgicale la plus utilisée pour le traitement de l'hypertrophie bénigne de la prostate. |
|
L'intervention enlève l'adénome par "rabotage" de la partie de la prostate obstruant le canal tout en laissant en place la "capsule prostatique" constituée par la glande normale refoulée en périphérie par l'adénome. L'intervention permet de traiter les prostates jusqu'à 60 ou 70 grammes, sous rachi-anesthésie ou anesthésie générale. L'intervention entraîne une éjaculation rétrograde dans 80 % des cas, mais les érections ne sont pas modifiées après l'intervention. Le risque d'incontinence post-opératoire est d'environ 2% et concerne surtout les patients de plus de 75 ans. Un rétrécissement urétral post-opératoire survient dans 2 à 3 % des cas. Le risque de réintervention est de 3 à 4 %.
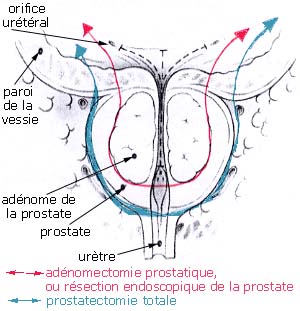
Schéma 8
|
|
Retour au sommaire |
|
4.4.1.3. Adénomectomie par voie haute.
|
|
En cas de gros adénome (supérieur à 70 g), l'intervention reste la classique adénomectomie par voie sus-pubienne. Les effets secondaires et les risques de cette intervention sont les mêmes que ceux de la résection endoscopique. Cette intervention faite pour adénome bénin laisse la "coque" prostatique, et ne doit pas être confondue avec la prostatectomie totale, faite pour cancer, qui enlève l'ensemble de la prostate (avec des conséquences différentes sur la continence urinaire et les érections). |
|
L'intervention par voie haute a prouvé son efficacité, car elle permet d'enlever parfaitement, jusqu'à la capsule chirurgicale, des adénomes même très volumineux. Le taux de réintervention est plus bas qu'en cas d'intervention endoscopique. |
|
|
La chirurgie ouverte est également préférée s'il existe, du fait de l'adénome, un calcul de vessie ne pouvant être fragmentée par voie endoscopique, un diverticule vésical volumineux nécessitant un traitement, une arthrose sévère des hanches (empêchant la résection). |
|
Retour au sommaire |
|
4.4.2. TRAITEMENTS INVASIFS ALTERNATIFS.
|
UroLift® :
une méthode simple et innovante pour traiter les symptômes urinaires de
l’adénome prostatique, sans effets secondaires sur l’éjaculation et les
érections
Le procédé UroLift®
est une option dans le traitement des symptômes du bas appareil urinaire
(SBAU) liés à une hypertrophie bénigne de la prostate chez les patients
intolérants à un traitement médical optimal, ou en cas de refus ou de
contre-indication aux autres traitements chirurgicaux endoscopique.
La procédure d'insertion de UroLift®
constitue une option intermédiaire pour les hommes hésitant entre l'option
thérapeutique et la résection transurétrale chirurgicale de la prostate
(TURP). UroLift® est plus
efficace que le médicament en termes d'efficacité, et a moins d’effets
secondaires, en particulier sexuels, que l’opération.
Principe
Le système UroLift®
a pour objectif de désobstruer l'urètre directement, sans aucune incision,
résection chirurgicale ni lésion par effet thermique, de la prostate. Les
lobes obstructifs prostatiques sont repoussés par les voies naturelles, puis
maintenus en place par de petits implants UroLift®
permanents, désobstruant ainsi l'urètre tout en laissant la prostate
intacte.
L’implant UroLift® est formé d’une languette capsulaire en nitinol reliée
par une suture en monofilament de polytétraphtalate d’éthylène (PET) à une
pièce terminale urétrale en acier inoxydable .Les implants sont posés grâce
à un dispositif à usage unique introduit dans l’urètre sous contrôle de la
vue. Le nombre d’implants à poser dépend du volume de la prostate, de la
longueur de l’urètre et du degré d’obstruction. En moyenne 4 implants sont
nécessaires.
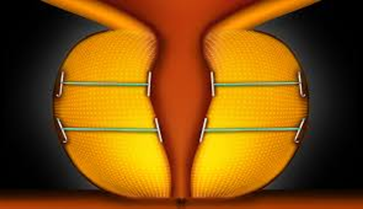
Voir la vidéo :
https://www.youtube.com/watch?v=cUZLA6txpUo
L’acte de pose peut être réalisé en chirurgie ambulatoire. Les modalités
anesthésiques sont l’anesthésie générale, l’anesthésie locorégionale
(rachianesthésie) ou surtout le plus
souvent une simple anesthésie locale.
Études cliniques
L’intérêt de UroLift® a été démontré par une vingtaine d’études dont 2
principales :
-
L’étude
multicentrique LIFT, contrôlée, randomisée, en simple aveugle réalisée
chez 206 patients avec un suivi de 5 ans (1). Elle a comparé la
symptomatologie et le débit urinaire après implantation du dispositif
UroLift® versus un traitement «fantôme» (procédure conduite à
l’identique sans les sutures des lobes prostatiques). Les patients 50 ans ou
plus, un score de symptômes IPSS > 12, un débit urinaire maximal
£ 12ml/s, et un volume prostatique entre 30 et 80 cc.
L’amélioration des symptômes a été rapide, 88% plus élevée après
UroLift® par rapport aux témoins dès 2 semaines après la mise
en place des implants. L’amélioration des symptômes, de la qualité de vie et
du débit urinaire a été durable après 5 ans, de 36%, 50% et 44%
respectivement. Le taux de retraitement sur 5 ans de suivi a été de
seulement 13,6%. Les effets secondaires ont été minimes et transitoires. La
fonction sexuelle (érection et
éjaculation) a été inchangée
par la mise en place des implants UroLift®.
- L’étude BPH-6 est une étude européenne
prospective,
multicentrique, contrôlée, randomisée, de non infériorité comparant
l’implant UroLift®
au traitement
chirurgical de référence, la résection endoscopique de
l’adénome de la prostate (RTUP). Au total, 80 patients ayant une hyperplasie
bénigne de la prostate (ou
adénome de la prostate) symptomatique ont été inclus dans l’étude réunissant
10 centres européens (2).
Une
amélioration significative des symptômes (score IPSS), de la qualité de vie,
et du débit urinaire a été observée dans les 2 groupes, sur la durée de 2
ans de l’étude. L’amélioration du débit et des symptômes a été supérieure
chez les patients opérés par RTUP, mais au prix d’une dégradation permanente
de la fonction sexuelle, et d’une moins bonne continence urinaire à 2
semaines et 3 mois après l’opération.
L’implant
UroLift® a permis une meilleure récupération post-opératoire et
une meilleure préservation du sommeil, du confort urinaire et des fonctions
sexuelles.
Les
résultats de l’ensemble des études montrent une efficacité du dispositif
UroLift® en termes d’amélioration de la symptomatologie de
l’hypertrophie bénigne de la prostate et de qualité de vie par rapport à un
dispositif « fantôme » et/ou par rapport à la valeur basale. Par ailleurs,
il a été observé une préservation de la fonction sexuelle (fonction
éjaculatoire et fonction érectile) après traitement par UroLift®.
Place dans la stratégie
thérapeutique
Dans les cas où les
patients sont en échec d’un traitement médicamenteux optimal et nécessitent
une chirurgie mais qu’ils ne peuvent en bénéficier (contre-indication ou
refus dans le but de préserver les fonctions sexuelles érectiles et
éjaculatoires), le dispositif UroLift® peut être proposé.
L’implantation se fait par une technique mini-invasive. Plusieurs implants
peuvent être posés au cours d’une même chirurgie en fonction du volume de la
prostate, de la longueur de l’urètre et du degré d’obstruction.
Au
vu des données, l’HAS a estimé que UroLift® a un intérêt dans la prise en charge des symptômes
urinaires liés à une hypertrophie bénigne de la prostate chez les patients
en échec d’un traitement médicamenteux optimal et/ou nécessitant une
chirurgie mais ne pouvant en bénéficier (contre-indication ou refus dans le but de préserver
les fonctions sexuelles érectiles et éjaculatoires).
La conclusion des études disponibles avec un recul maximum de 5 ans est que
UroLift®
permet une diminution significative
de la gêne urinaire et des symptômes. L’HAS a trouvé un intérêt
thérapeutique à UroLift®
au regard de la préservation des fonctions sexuelles (érectiles et
éjaculatoires) qu’il permet.
L’implantation d’UroLift® est
soumise au respect des critères suivants:
-chirurgie programmée, non réalisée dans l’urgence.
-homme d’âge > 50 ans
-HBP
symptomatique non compliquée (exclusion des patients avec une insuffisance
rénale obstructive, rétention vésicale complète, lithiase vésicale)
-volume prostatique inférieur à 80 cc
-patients n’ayant pas d’antécédent de chirurgie prostatique
-absence d’infection urinaire
-mesure de l’échec ou de l’intolérance au traitement médical bien conduit
par l’évaluation de l’aggravation de la gêne liée aux symptômes du bas
appareil urinaire par un auto-questionnaire patient standardisé urinaire et
par une débitmétrie
-urétrocystoscopie diagnostique pour vérifier la faisabilité du
geste, l’absence de pathologie urétro-vésicale associée et éliminer une
hypertrophie de la partie médiane de la prostate (lobe médian ou protrusion
intra-vésicale).
A l'inverse de toutes les
autres options thérapeutiques permanentes pour le traitement de
l'hyperplasie de la prostate, cette procédure mini-invasive d'insertion d'un
implant UroLift®
dure généralement moins d'une heure et peut-être réalisée sous anesthésie
locale. Le patient peut ainsi rentrer chez lui peu de temps après.
En France, l’HAS a émis
en 2017 une recommandation positive pour son utilisation et son
remboursement (3).
Le système est notamment
proposé aux patients à la Fondation St Jean de Dieu-Oudinot à Paris (Pr
Flam), et à l’hôpital de Bordeaux (Dr Robert), de Montpellier (Dr Maxime
Robert), de Lille et de Lyon Sud (Pr Ruffion).. D’autres centres seront
ouverts en France fin 2019.
Références
1-
Roehrborn CG et al. Five
year results of the prospective randomized controlled prostatic urethral
L.I.F.T. study. Can J Urol 2017;24(3): 8802-8813.
2-
Gratzke C. et al.
Prostatic urethral lift vs transurethral resection
of the prostate: 2-year results of the BPH6 prospective, multicentre,
randomized study.
BJU Int 2017; 119: 767–775
3-
https://www.has-sante.fr/portail/upload/docs/evamed/CEPP-5303_urolift_30_mai_2017_(5303)_avis.pdf
- Résection prostatique par laser : Les indications de
la résection prostatique par laser sont limitées par les effets secondaires
irritatifs qui durent plus longtemps qu’après une résection classique ou par
courant bipolaire ; et par la durée et le caractère fastidieux de
l’opération. Ce type de traitement a des indications surtout chez les
patients ayant un trouble de la coagulation ou chez qui on ne peut arrêter
le traitement anti coagulant. Le laser Greenlight® est le
plus souvent utilisé pour la vaporisation du tissu prostatique.
Le
laser Holmium est utilisé dans les volumineux adénomes pour
faire une énucléation de l’adénome qui est ensuite morcelé dans la vessie.
Une toute nouvelle technique en plein développement est
l’énucléation par plasma ou courant bipolaires (B-TUEP). Plus
simple à mettre en œuvre que son homologue utilisant un laser, elle permet
d’obtenir d’excellents résultats fonctionnels dans le traitement des gros
adénomes. Cette approche a été validée dans des études, y compris
randomisées, montrant l’efficacité fonctionnelle et le faible taux d’effets
secondaires (1,2).
1 Giulianelli R1,
Gentile BC2, Mirabile G1, Albanesi L1, Tariciotti P1, Rizzo G1, Buscarini
M3, Falavolti C4. Bipolar Plasma Enucleation of the Prostate (B-TUEP) in
Benign Prostate Hypertrophy Treatment. 3-Year Results". Urology. 2017 May
30.
2 Geavlete B, Stanescu F, Iacoboaie C, Geavlete P. Bipolar plasma
enucleation of the prostate vs open prostatectomy in large benign prostatic
hyperplasia cases - a medium term, prospective, randomized comparison. BJU
Int. 2013 May ;111(5) :793-803
- Endoprothèse urétrale ("stent") :
Il s'agit de tubes, plastiques ou métalliques, placés au niveau de l'urètre
prostatique, maintenus en place par la pression de la glande, et qui
maintiennent perméable la lumière urétrale. Ces prothèses sont utilisées en
cas de contre-indication chirurgicale absolue (accident vasculaire cérébral
ou infarctus récents). Les complications sont la migration, l'infection et
les calcifications qui surviennent après un délai variable. Ces techniques
ont été quasi abandonnées.
- Thermothérapie :
L'élément actif est en général un système à micro-ondes. La thermothérapie
élève la température du tissu prostatique à plus de 45° et peut créer une
nécrose tissulaire définitive. Cette nécrose est théoriquement remplacée par
du tissu conjonctif qui se rétracte secondairement, aboutissant à une
diminution du volume prostatique. La technique est peu utilisée, car plutôt
inefficace. PROSTIVA® ou TUNA® : ce système permet une
élévation de la température prostatique par micro-ondes, ce qui entraîne une
coagulation et une rétraction du tissu prostatique. Il est très peu utilisé.
Le système Rezūm utilise de la vapeur d’eau injectée
dans la prostate par voie endoscopique, pour créer une nécrose de
coagulation et diminuer l’adénome.
|
|
|
|
Retour au sommaire |
|
4.4.3. TRAITEMENT MEDICAL.
|
|
Les années récentes ont été marquées par
une diminution notable du nombre d'interventions chirurgicales faites pour
adénome. Cette diminution observée dans tous les pays développés peut
atteindre plus de 40 % par an dans certains cas. Cette évolution
s'explique par l'apparition de traitements médicaux efficaces et par
l'attirance des patients vers ces solutions non chirurgicales.
En l'absence de complications
nécessitant un traitement chirurgical, le traitement médical de l'adénome
dépend essentiellement de la gêne causée par les symptômes et de l'impact
sur la qualité de vie du patient.
La simple surveillance annuelle,
le traitement par alpha-bloquants et le traitement par inhibiteur de la 5
alpha-réductase sont actuellement les options thérapeutiques dont
l’efficacité a été démontrée par des études prospectives à long terme (> 1
an) randomisées avec un groupe placebo.
LES MEDICAMENTS DE L'ADENOME PROSTATIQUE
Inhibiteur de la 5 alpha-réductase
Finastéride :CHIBRO-PROSCAR®
5 mg 1 cp/jour
Dutastéride : AVODART® 1 cp/jour
Extrait de plantes
Serenoa
repens : PERMIXON® 1 x 2 fois/jour
Pygeum africanum : TADENAN®
50 mg 1 x 2 fois/jour
Alpha bloquants
Térazosine : DYSALFA® 5 mg (titration nécessaire) :
1 le soir
HYTRINE® 5mg
(titration nécessaire) : 1 le soir
Alfuzosine : XATRAL® 2,5 mg :
3 cps/jour
URION® 2,5 mg : 3
cps/jour
XATRAL® LP
10 : 1 cp le soir
Doxazosine : ZOXAN® 8mg : 1 cp le soir
ZOXAN® 4 mg : 1 cp le soir
Alpha 1- a bloquant
Tamsulosine : OMIX®
JOSIR®
OMEXEL®
MECIR® : 1 cp / jour
Silodosine :
SILODYX® 4 ou 8 mg : 1 cp le soir
UROREC® 4 ou 8 mg : 1 cp le soir
Combinaisons
Tamsulosine+Dutastéride : COMBODART® : 1 cp
le soir
|
|
|
Retour au sommaire |
|
4.4.3.1. Les différents médicaments utilisés dans l'HBP.
|
|
- Alpha-bloquants :
Ils agissent par blocage des récepteurs alpha-1
situés au niveau du trigone vésical, de l'urètre et de la prostate,
entraînant une relaxation du col vésical, et des fibres musculaires lisses
intra prostatiques. Les alpha-bloquants sont utilisés soit chez des
patients présentant une HBP symptomatique plutôt sévère (rétention
chronique marquée, infections à répétition ...), soit chez des patients
plutôt jeunes dont les troubles sont plus liés à une maladie du col qu'à
l'hypertrophie prostatique.
Effets indésirables : surtout hypotension
orthostatique et vertiges, obligeant à l’arrêt du traitement dans 10-15 %
des cas.
La tamsulosine agit par blocage des récepteurs alpha-1-a,
spécifiques de la prostate. Ce blocage sélectif permettrait d’éviter les
effets secondaires vasculaires.. L'effet de la tamsulosine sur la pression
artérielle systolique et diastolique est négligeable, mais parfois
palpitations, éjaculation rétrograde.
- Inhibiteurs de la
5-alpha réductase :
La 5-alpha réductase est l’enzyme qui
transforme la testostérone en DHT dans la prostate. Le traitement induit
une diminution du volume prostatique, et une amélioration progressive des
symptômes cliniques. Il permet de diminuer la fréquence de la rétention
urinaire aiguë, le recours à une intervention chirurgicale. Les troubles
de l'érection sont plus fréquents sous finastéride (19 % contre 10 % en
cas de placebo). Le traitement par finastéride CHIBRO-PROSCAR® ou AVODART®
peut renverser la progression naturelle de l'adénome.
L’effet clinique
est d’autant plus net que la prostate est plus volumineuse (> 40 g)
initialement, et il se maintient dans le temps. Ainsi,
à long terme, l’inhibiteur de la
5-alpha réductase est capable de modifier le cours naturel de la maladie.
Les données à 6 ans du Chibro-Proscar® (extension ouverte de l’étude
PLESS) ont confirmé les résultats sur la diminution de l’incidence de la
rétention urinaire aiguë et/ou du recours à la chirurgie (1). L’Avodart®
entraîne, sur 2 ans, une diminution du volume d’environ 25%, une
diminution du risque de rétention aiguë de 57% et une réduction du recours
à la chirurgie de 48% (2).
Sous Chibro-Proscar®, le taux de PSA est
diminué par 2. Après 6 mois de traitement, il faut donc multiplier le taux
par 2 pour connaître le taux théorique du patient. Avec cette règle, la
valeur du PSA pour le diagnostic de cancer de la prostate n’est pas
modifiée.
1 Roehrborn CG et
al, Sustained decrease in incidence of acute urinary retention and surgery
with finasteride for 6 years in men with benign prostatic hyperplasia. J
Urol. 171:1194, 2004
2 Roehrborn CG et al for ARIA3001 ARIA3002 and
ARIA3003 Study Investigators. Efficacy and safety of a dual inhibitor of
5-alpha-reductase types 1 and 2 (dutasteride) in men with benign prostatic
hyperplasia.
Urology. 60:434, 2002
- Inhibiteurs de la phosphodiestérase :
ces médicaments, en
particulier le Cialis5® utilisé pour les troubles de l’érection, peuvent
être aussi utilisés pour améliorer les troubles urinaires de l’HBP.
Leur réelle efficacité dans cette indication est cependant controversée,
et leur prix est un frein à leur utilisation dans ce domaine.
- Extraits de plantes :
Leur mode d’action éventuel est
inconnu. Malgré leur utilisation depuis de nombreuses années, il n'y a pas
d’études prospectives à long terme contre placebo montrant l’efficacité de
cette classe thérapeutique.
Seuls les alpha-bloquants et le
finastéride ont montré à ce jour, dans des études cliniques menées selon
les recommandations de l’ANDEM et de la conférence internationale de
Consensus, qu’ils peuvent améliorer significativement les symptômes chez
les patients.
Les indications respectives de ces deux classes
thérapeutiques considérées comme efficaces dans le traitement de l'adénome
symptomatique sont progressivement définies par les études cliniques.
- Dans le traitement de l'adénome,
l'association de 2 médicaments paraît bénéfique.
L'association
de deux médicaments de l'adénome prostatique ayant des modes d'action
différents est un concept qui a fait l'objet d'une étude récente.
L'intérêt potentiel est d'associer 2 médicaments agissant selon des modes
d'action différents mais complémentaires: un alpha-bloquant agissant
rapidement sur le tonus des fibres musculaires lisses de le prostate d'une
part, et un inhibiteur de la 5 alpha réductase agissant à plus long terme
en diminuant le volume de la prostate d'autre part.
L'étude
MTOPS (Medical Therapy of Prostatic Symptoms) a comparé à un placebo
l'association du finastéride (CHIBRO-PROSCAR®) et d'un alpha-1-bloquant
(ZOXAN® ou doxazosine), pendant une durée moyenne de 4,5 ans. Par rapport
au placebo, l'association des 2 médicaments a diminué le risque de
progression de l'adénome de 67 %, le risque de rétention urinaire de 79 %,
et le risque d'opération chirurgicale de 69 % (1). Cette étude suggère
donc un avantage à l'association de 2 médicaments complémentaires pour
traiter l'adénome de la prostate.
De même, l’étude CombAT a
étudié la combinaison dutastéride et tamsulosine. Cette étude prospective
randomisée en double aveugle sur une durée de 4 ans a montré une réduction
significative du risque de rétention urinaire aiguë et de recours à la
chirurgie par rapport à la tamsulosine seule; et une amélioration
significative des symptômes par rapport aux deux médicaments pris seuls.
Un médicament
(Combodart®) associe les 2 molécules,
Référence:
McConnell J.D. The long-term effect of doxazosin,
finasteride, and combination therapy on the clinical progression of benign
prostatic hyperplasia. N Engl J Med.349: 2387, 2003
|
|
Retour au sommaire |
|
4.5. COMMENT DECIDER DU TRAITEMENT THERAPEUTIQUE DANS L’ADENOME ?
|
|
En dehors des indications formelles de la chirurgie, les indications dépendent surtout de la gêne fonctionnelle due aux symptômes. Pour une symptomatologie identique, cette gêne est variable selon les patients. Si les symptômes sont ressentis comme gênants par le patient, un traitement est indiqué. Le seul volume prostatique, même important, ne constitue pas une indication à un traitement. |
|
La tendance des patients est de choisir le traitement le moins agressif et le moins susceptible d'entraîner des complications, même si l'efficacité est moindre. . Une discussion entre le patient et le médecin est primordiale pour évaluer les troubles et décider du traitement le mieux adapté. |
|
Retour au sommaire |
|
4.5.1. Il existe des cas où le traitement chirurgical est indiscutable.
|
|
- rétention aiguë non médicamenteuse |
|
(après l'échec d'une tentative d'ablation de sonde) |
|
- dilatation des reins obstructive avec ou sans insuffisance rénale |
|
- hématurie (sang dans les urines) |
|
- infections urinaires à répétition |
|
- calcul vésical |
|
- symptômes sévères non améliorés par un traitement médical |
|
Retour au sommaire |
|
4.5.2. Les indications, en dehors d’une indication chirurgicale formelle, dépendent du bilan initial ET DE LA GENE RESSENTIE PAR LE PATIENT.
|
| Si les examens sont normaux et la gène minime, on propose une simple surveillance, et le même bilan est refait tous les ans chez les patients de plus de 50 ans. |
|
| Si les examens sont normaux et les symptômes gênants, un traitement est proposé au patient. Ce traitement sera d'abord médical, et le type de traitement choisi en fonction du patient (âge, terrain), et de l'efficacité et des effets secondaires de chaque médicament. |
|
Retour au sommaire |






